镍镉/镍氢电池的发展
1899年,Waldmar Jungner在开口型镍镉电池中,首先使用了镍极板,几乎与此同时,Thomas Edison 发明了用于电动车的镍铁电池。遗憾的是,由于当时这些碱性蓄电池的极板材料比其它蓄电池的村料贵得多,因此实际应用受到了极大的限制。
后来,Jungner的镍镉电池经过几次重要改进,性能明显改善。其中最重要的改进是在1932年,科学家在镍电池中开始使用了活性物质。他们将活性物质放入多孔的镍极板中,然后再将镍极板装入金属壳内。镍镉电池发展史上另一个重要的里程碑是1947年密封型镍镉电池研制成功。在这种电池中,化学反应产生的各种气体不用排出,可以在电池内部化合。密封镍镉电池的研制成功,使镍镉电池的应用范围大大增加。
密封镍镉电池效率高、循环寿命长、能量密度大、体积小、重量轻、结构紧凑,并且不需要维护,因此在工业和消费产品中得到了广泛应用。
随着空间技术的发展,人们对电源的要求越来越高。70年代中期,美国研制成功了功率大、重量轻、寿命长、成本低的镍氢电池,并且于1978年成功地将这种电池应用在导航卫星上,镍氢电池与同体积镍镉电池相比,容量可提高一倍,而且没有重金属镉带来的污染问题。它的工作电压与镍镉电池完全相同,工作寿命也大体相当,但它具有良好的过充电和过放电性能。近年来,镍氢电池受到世界各国的重视,各种新技术层出不穷。镍氢电池刚问世时,要使用高压容器储存氢气,后来人们采用金属氢化物来储存氢气,从而制成了低压甚至常压镍氢电池。1992年,日本三洋公司每月可生产200万只镍氢电池。目前国内已有20多个单位研制生产镍氢电池,国产镍氢电池的综合性能已经达到国际先进水平。
蓄电池参数
蓄电池的五个主要参数为:电池的容量、标称电压、内阻、放电终止电压和充电终止电压。电池的容量通常用Ah(安时)表示,1Ah就是能在1A的电流下放电 1小时。单元电池内活性物质的数量决定单元电池含有的电荷量,而活性物质的含量则由电池使用的材料和体积决定,因此,通常电池体积越大,容量越高。与电池容量相关的一个参数是蓄电池的充电电流。蓄电池的充电电流通常用充电速率C表示,C为蓄电池的额定容量。例如,用2A电流对1Ah电池充电,充电速率就是 2C;同样地,用2A电流对500mAh电池充电,充电速率就是4C。
电池刚出厂时,正负极之间的电势差称为电池的标称电压。标称电压由极板材料的电极电位和内部电解液的浓度决定。当环境温度、使用时间和工作状态变化时,单元电池的输出电压略有变化,此外,电池的输出电压与电池的剩余电量也有一定关系。单元镍镉电池的标称电压约为1.3V(但一般认为是1.25V),单元镍氢电池的标称电压为1.25V。
电池的内阻决定于极板的电阻和离子流的阻抗。在充放电过程中,极板的电阻是不变的,但是,离子流的阻抗将随电解液浓度的变化和带电离子的增减而变化。
蓄电池充足电时,极板上的活性物质已达到饱和状态,再继续充电,蓄电池的电压也不会上升,此时的电压称为充电终止电压。镍镉电池的充电终止电压为1.75~1.8V,镍氢电池的充电终止电压为1.5V。
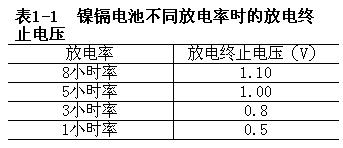
表1-1 镍镉电池不同放电率时的放电终止电压
放电终止电压是指蓄电池放电时允许的最低电压。如果电压低于放电终止电压后蓄电池继续放电,电池两端电压会迅速下降,形成深度放电,这样,极板上形成的生成物在正常充电时就不易再恢复,从而影响电池的寿命。放电终止电压和放电率有关。镍镉电池的放电终止电压和放电速率的关系如表1-1所列,镍氢电池的放电终止电压一般规定为1V。
镍镉蓄电池的工作原理
镍镉蓄电池的正极材料为氢氧化亚镍和石墨粉的混合物,负极材料为海绵状镉粉和氧化镉粉,电解液通常为氢氧化钠或氢氧化钾溶液。当环境温度较高时,使用密度为1.17~1.19(15℃时)的氢氧化钠溶液。当环境温度较低时,使用密度为1.19~1.21(15℃时)的氢氧化钾溶液。在-15℃以下时,使用密度为1.25~1.27(15℃时)的氢氧化钾溶液。为兼顾低温性能和荷电保持能力,密封镍镉蓄电池采用密度为1.40(15℃时)的氢氧化钾溶液。为了增加蓄电池的容量和循环寿命,通常在电解液中加入少量的氢氧化锂(大约每升电解液加15~20g)。
镍镉蓄电池充电后,正极板上的活性物质变为氢氧化镍〔NiOOH〕,负极板上的活性物质变为金属镉;镍镉电池放电后,正极板上的活性物质变为氢氧化亚镍,负极板上的活性物质变为氢氧化镉。
1.放电过程中的电化学反应
(1)负极反应
负极上的镉失去两个电子后变成二价镉离子Cd2+,然后立即与溶液中的两个氢氧根离子OH-结合生成氢氧化镉Cd(OH)2,沉积到负极板上。
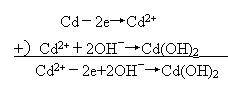
(2)正极反应
正极板上的活性物质是氢氧化镍(NiOOH)晶体。镍为正三价离子(Ni3+),晶格中每两个镍离子可从外电路获得负极转移出的两个电子,生成两个二价离子2Ni2+。与此同时,溶液中每两个水分子电离出的两个氢离子进入正极板,与晶格上的两个氧负离子结合,生成两个氢氧根离子,然后与晶格上原有的两个氢氧根离子一起,与两个二价镍离子生成两个氢氧化亚镍晶体。
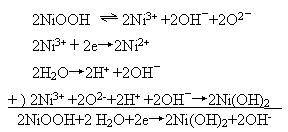
将以上两式相加,即得镍镉蓄电池放电时的总反应:
2.充电过程中的化学反应
充电时,将蓄电池的正、负极分别与充电机的正极和负极相连,电池内部发生与放电时完全相反的电化学反应,即负极发生还原反应,正极发生氧化反应。
(1)负极反应
充电时负极板上的氢氧化镉,先电离成镉离子和氢氧根离子,然后镉离子从外电路获得电子,生成镉原子附着在极板上,而氢氧根离子进入溶液参与正极反应:
(2) 正极反应
在外电源的作用下,正极板上的氢氧化亚镍晶格中,两个二价镍离子各失去一个电子生成三价镍离子,同时,晶格中两个氢氧根离子各释放出一个氢离子,将氧负离子留在晶格上,释出的氢离子与溶液中的氢氧根离子结合,生成水分子。然后,两个三价镍离子与两个氧负离子和剩下的二个氢氧根离子结合,生成两个氢氧化镍晶体:
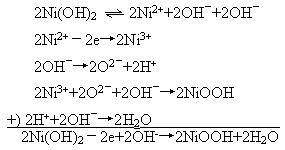
将以上两式相加,即得镍镉蓄电池充电时的电化学反应:
蓄电池充电终了时,充电电流将使电池内发生分解水的反应,在正、负极板上将分别有大量氧气和氢气析出,其电化学反应如下:
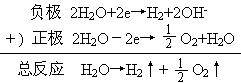
从上述电极反应可以看出,氢摒化钠或氢氧化钾并不直接参与反应,只起导电作用。从电池反应来看,充电过程中生成水分子,放电过程中消耗水分子,因此充、放电过程中电解液浓度变化很小,不能用密度计检测充放电程度。
3. 端电压
充足电后,立即断开充电电路,镍镉蓄电池的电动势可达1.5V左右,但很快就下降到1.31-1.36V。
镍镉蓄电池的端电压随充放电过程而变化,可用下式表示:
U充=E充+I充R内
U放=E放-I放R内
从上式可以看出,充电时,电池的端电压比放电时高,而且充电电流越大,端电压越高;放电电流越大,端电压越低。
当镍镉蓄电池以标准放电电流放电时,平均工作电压为1.2V。采用8h率放电时,蓄电池的端电压下降到1.1V后,电池即放完电。
4. 容量和影响容量的主要因素
蓄电池充足电后,在一定放电条件下,放至规定的终止电压时,电池放出的总容量称为电池的额定容量,容量Q用放电电流与放电时间的乘积来表示,表示式如下:
Q=I·t(Ah)
镍镉蓄电池容量与下列因素有关:
① 活性物质的数量;
② 放电率;
③ 电解液。
放电电流直接影响放电终止电压。在规定的放电终止电压下,放电电流越大,蓄电池的容量越小。
使用不同成分的电解液,对蓄电池的容量和寿命有一定的影响。通常,在高温环境下,为了提高电池容量,常在电解液中添加少量氢氧化锂,组成混合溶液。实验证明:每升电解液中加入15~20g含水氢氧化锂,在常温下,容量可提高4%~5%,在40℃时,容量可提高20%。然而,电解液中锂离子的含量过多,不仅使电解液的电阻增大,还会使残留在正极板上的锂离子(Li+)慢慢渗入晶格内部,对正极的化学变化产生有害影响。
电解液的温度对蓄电池的容量影响较大。这是因为随着电解液温度升高,极板活性物质的化学反应也逐步改善。
电解液中的有害杂质越多,蓄电池的容量越小。主要的有害杂质是碳酸盐和硫酸盐。它们能使电解液的电阻增大,并且低温时容易结晶,堵塞极板微孔,使蓄电池容量显著下降。此外,碳酸根离子还能与负极板作用,生成碳酸镉附着在负极板表面上,从而引起导电不良,使蓄电池内阻增大,容量下降。
5. 内阻
镍镉蓄电池的内阻与电解液的导电率、极板结构及其面积有关,而电解液的导电率又与密度和温度有关。电池的内阻主要由电解液的电阻决定。氢氧化钾和氢氧化钠溶液的电阻系数随密度而变。18℃时氢氧化钾溶液和氢氧化钠溶液的电阻系数最小。通常镍镉蓄电池的内阻可用下式计算:
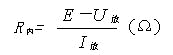
6. 效率与寿命
在正常使用的条件下,镍镉电池的容量效率ηAh为67%-75%,电能效率ηWh为55%~65%,循环寿命约为2000次。容量效率ηAh和电能效率ηWh计算公式如下:
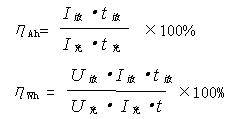
(U充和U放应取平均电压)
7. 记忆效应
镍镉电池使用过程中,如果电量没有全部放完就开始充电,下次再放电时,就不能放出全部电量。比如,镍镉电池只放出80%的电量后就开始充电,充足电后,该电池也只能放出80%的电量,这种现象称为记忆效应。
电池全部放完电后,极板上的结晶体很小。电池部分放电后,氢氧化亚镍没有完全变为氢氧化镍,剩余的氢氧化亚镍将结合在一起,形成较大的结晶体。结晶体变大是镍镉电池产生记忆效应的主要原因。
镍氢电池的工作原理
镍氢电池和同体积的镍镉电池相比,容量增加一倍,充放电循环寿命也较长,并且无记忆效应。镍氢电池正极的活性物质为NiOOH(放电时)和Ni(OH)2 (充电时),负极板的活性物质为H2(放电时)和H2O(充电时),电解液采用30%的氢氧化钾溶液,充放电时的电化学反应如下:

从方程式看出:充电时,负极析出氢气,贮存在容器中,正极由氢氧化亚镍变成氢氧化镍(NiOOH)和H2O;放电时氢气在负极上被消耗掉,正极由氢氧化镍变成氢氧化亚镍。
过量充电时的电化学反应:

从方程式看出,蓄电池过量充电时,正极板析出氧气,负极板析出氢气。由于有催化剂的氢电极面积大,而且氢气能够随时扩散到氢电极表面,因此,氢气和氧气能够很容易在蓄电池内部再化合生成水,使容器内的气体压力保持不变,这种再化合的速率很快,可以使蓄电池内部氧气的浓度,不超过千分之几。
从以上各反应式可以看出,镍氢电池的反应与镍镉电池相似,只是负极充放电过程中生成物不同,从后两个反应式可以看出,镍氢电池也可以做成密封型结构。镍氢电池的电解液多采用KOH水溶液,并加入少量的LiOH。隔膜采用多孔维尼纶无纺布或尼龙无纺布等。为了防止充电过程后期电池内压过高,电池中装有防爆装置。
电池充电特性
镍镉电池充电特性曲线如图1所示。当恒定电流刚充入放完电的电池时,由于电池内阻产生压降,所以电池电压很快上升(A点)。此后,电池开始接受电荷,电池电压以较低的速率持续上升。在这个范围内(AB之间),电化学反应以一定的速率产生氧气,同时氧气也以同样的速率与氢气化合,因此,电池内部的温度和气体压力都很低。
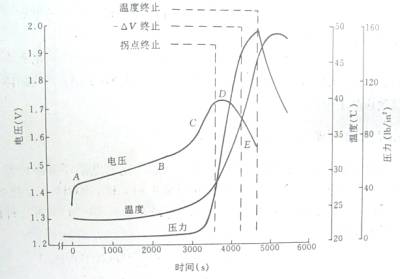
图 1 镍镉电池的充电曲线
电池充电过程中,产生的氧气高于复合的氧气时,电池内压力升高。电池内的正常压力*大约为1磅力/英寸2。过充电时,根据充电速率,电池内部压力将很快上升到100磅力/英寸2或者更高。
研究蓄电池的各种充电方法时,镍镉电池内产生的气体是一个重要问题。气泡聚集在极板表面,将减小极板表面参与化学反应的面积并且增加电池的内阻。过充电时,电池内产生的大量气体,如果不能很快复合,电池内部的压力就会显著增加,这样将损伤电池。此外,压力过大时,密封电池将打开放气孔,从而使电解液逸散。若电解液反复通过放气孔逸散,电解液的粘稠性增大,极板间离子的传输变得困难,因此电池的内阻增加,容量下降。
经过一定时间后(C点),电解液中开始产生气泡,这些气泡聚集在极板表面,使极板的有效面积减小,所以电池的内阻抗增加,电池电压开始较快上升。这是接近充足电的信号。
充足电后,充入电池的电流不是转换为电池的贮能,而是在正极板上产生氧气超电位。氧气是由于电解液电解而产生的,不是由于氢氧化镉还原为镉而产生的。在氢氧化钾和水组成的电解液中,氢氧离子变成氧、水和自由电子,反应式为 4OH?D→O2↑+2H2O+4e?D
虽然电解液产生的氧气能很快在负极板表面的电解液中复合,但是电池的温度仍显著升高。此外由于充电电流用来产生氧气,所以电池内的压力也升高。
由于从大量的氢氧离子中比从很少的氢氧化镉中更容易分解出氧气,所以电池内的温度急剧上升,这样就使电池电压下降。因此电池电压曲线出现峰值(D点)。
电解液中,氧气的产生和复合是放热反应,电池过充电时(E点),不停地产生氧气,从而使电池内的温度和压力升高。如果强制排出气体,将引起电解液减少、电池容量下降并损伤电池。若气体不能很快排出,电池将会爆炸。
采用低速率恒流涓流充电时,电池内将产生枝晶。这些枝晶能够通过隔板在极板之间扩散。在扩散较严重的情况下,这些枝晶会造成电池部分或全部短路。
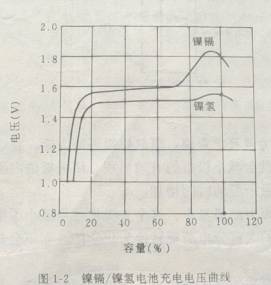
镍氢电池的充电特性与镍镉电池类似,充电过程中二者的电压、温度曲线如图1-2和图1-3所示。可以看出,充电终止时,镍镉电池电压下降比镍氢电池要大得多。当电池容量达到额定容量的80%以前,镍镉电池的温度缓慢上升,当电池容量达到90%以后,镍镉电池的温度才很快上升。当电池基本充足电时,镍镉/镍氢电池的温度上升率基本相同。
充电过程与充电方法
电池的充电过程通常可分为预充电、快速充电、补足充电、涓流充电四个阶段。
对长期不用的或新电池充电时,一开始就采用快速充电,会影响电池的寿命。因此,这种电池应先用小电流充电,使其满足一定的充电条件,这个阶段称为预充电。
快速充电就是用大电流充电,迅速恢复电池电能。快速充电速率一般在1C以上,快速充时间由电池容量和充电速率决定。
为了避免过充电,一些充电器采用小电流充电。镍镉电池正常充电时,可以接受C/10或更低的充电速率,这样充电时间要10h以上。采用小电流充电,电池内不会产生过多的气体,电池温度也不会过高。只要电池接到充电器上,低速率恒流充电器就能对电池提供很小的涓流充电电流。电池采用小电流充电时,电池内产生的热量可以自然散去。
涓流充电器的主要问题是充电速度太慢,例如,容量为1Ah的电池,采用C/10充电速率时,充电时间要10h以上。此外,电池采用低充电速率反复充电时,还会产生枝晶。大部分涓流充电器中,都没有任何电压或温度反馈控制,因而不能保证电池充足电后,立即关断充电器。
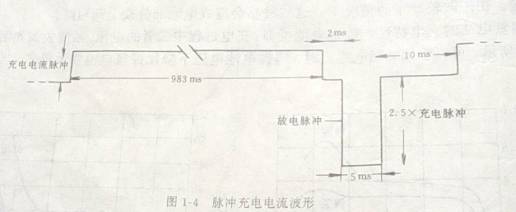
快速充电分恒流充电和脉冲充电两种,恒流充电就是以恒定电流对电流充电,脉冲充电则是首先用脉冲电流对电池充电。然后让电池放电,如此循环。电池脉冲的幅值很大、宽度很窄。通常放电脉冲的幅值为充电脉冲的3倍左右。虽然放电脉冲的幅值与电池容量有关,但是,与充电电流幅值的比值保持不变,脉冲充电时,充电电流波形如图1-4所示。
充电过程中,镍镉电池中的氢氧化镍还原为氢氧化亚镍,氢氧化镉还原为镉。在这个过程中产生的气泡,聚集在极板两边,这样就会减小极板的有效面积,使极板的内阻增大。由于极板的有效面积变小,充入全部电量所需的时间增加。
加入放电脉冲后,气泡离开极板并与负极板上的氧复合。这个去极化过程减小了电池的内部压力、温度和内阻。同时,充入电池的大部分电荷都转换为化学能,而不会转变为气体和热量。
充放电脉冲宽度的选择应能保证极板恢复原来的晶体结构,从而消除记忆效应。采用放电去极化措施后,可以提高充电效率并且允许大电流快速充电。





 返回顶部
返回顶部 刷新页面
刷新页面 下到页底
下到页底