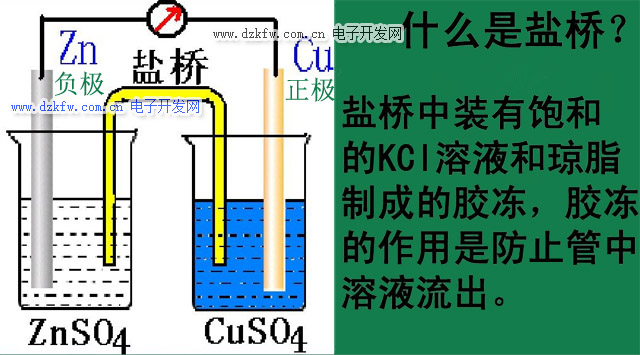
什么是盐桥,盐桥作用原理
盐桥是为了减小液接电位,转移离子而在两种溶液之间连接的高浓度电解质溶液。盐桥常出现在原电池中,是由琼脂和饱和氯化钾或饱和硝酸钾溶液构成的。
盐桥作用原理
在两种溶液之间插入盐桥以代替原来的两种溶液的直接接触,减免和稳定液接电位(当组成或活度不同的两种电解质接触时,在溶液接界处由于正负离子扩散通过界面的离子迁移速度不同造成正负电荷分离而形成双电层,这样产生的电位差称为液体接界扩散电位,简称液接电位),使液接电位减至最小以致接近消除。 防止试液中的有害离子扩散到参比电极的内盐桥溶液中影响其电极电位。
饱和KCl溶液的浓度高达4.2mol・dm-3,当盐桥插入到浓度不大的两电解质溶液之间的界面时,产生了两个接界面,盐桥中K+和Cl-向外扩散就成为这两个接界面上离子扩散的主流。由于K+和Cl-的扩散速率相近,使盐桥与两个溶液接触产生的液接电势均很小,且两者方向相反,故相互抵消后降至1~2mV。选择盐桥中的电解质的原则是高浓度、正负离子迁移数接近相等,且不与电池中溶液发生化学反应。常采用KCl、NH4NO3和KNO3的饱和溶液。
为什么带有盐桥的和不带有盐桥的原电池电流持续时比较分析?
带有盐桥的和不带有盐桥的原电池,带有盐桥的持续时间更长:
1、有盐桥的原电池中盐桥原电池中,还原剂在负极区,而氧化剂在正极区,化学能转化成了电能,电流稳定,且持续时间长。
2、而没有盐桥的的原电池比有盐桥的原电池:效率较低,温度会变,产生的电流较不稳定。因此,没有盐桥的的原电池比有盐桥的原电池:效率较低,温度会变,产生的电流较不稳定。
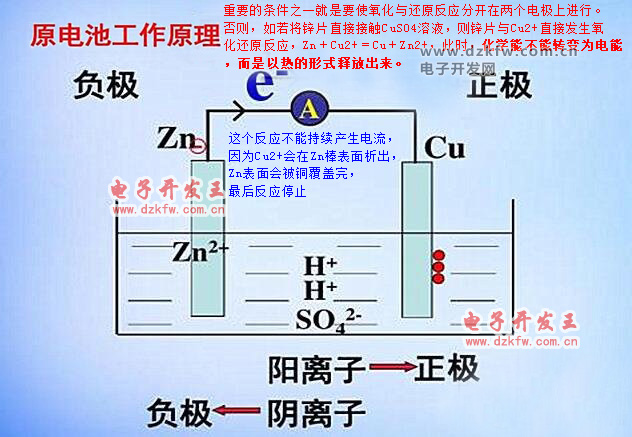
原电池反应属于放热的反应,一般是氧化还原反应。
但区别于一般的氧化还原反应的是,电子转移不是通过氧化剂和还原剂之间的有效碰撞完成的,而是还原剂在负极上失电子发生氧化反应,电子通过外电路输送到正极上,氧化剂在正极上得电子发生还原反应,从而完成还原剂和氧化剂之间电子的转移。
两极之间溶液中离子的定向移动和外部导线中电子的定向移动构成了闭合回路,使两个电极反应不断进行,发生有序的电子转移过程,产生电流,实现化学能向电能的转化。
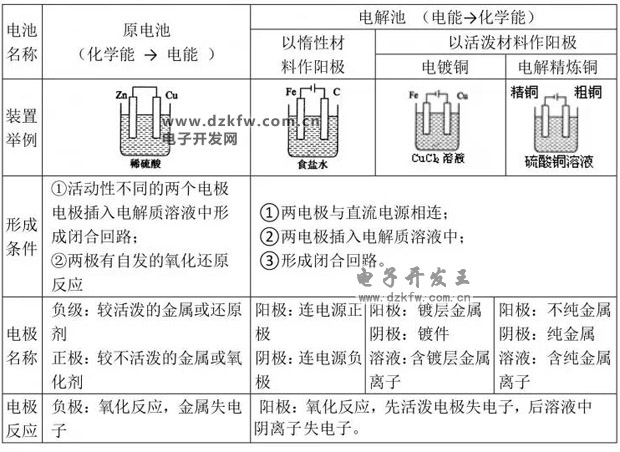
原电池形成条件
1、电极材料由两种金属活泼性不同的金属或由金属与其他导电的材料(非金属或某些氧化物等)组成。
2、电解质存在。
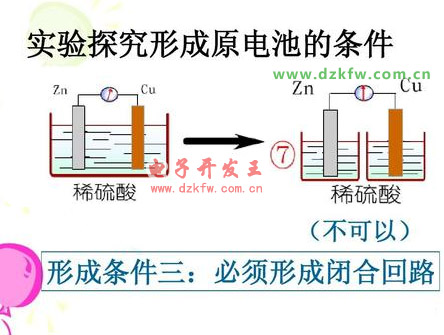
3、两电极之间有导线连接,形成闭合回路。
4、发生的反应是自发的氧化还原反应。
只要具备前三个条件就可构成原电池。而化学电源因为要求可以提供持续而稳定的电流,所以除了必须具备原电池的三个构成条件之外,还要求有自发进行的化学反应。也就是说,化学电源必须是原电池,但原电池不一定都能做化学电池。



 返回顶部
返回顶部 刷新页面
刷新页面 下到页底
下到页底