电解池原理
(1)电解:使电流通过电解质溶液且在阴、阳极两极引起氧化还原反应的过程叫电解。
(2)装置:电解池(电解槽)
(3)特点:将电能转化为化学能。
形成条件:①与电源相连的两个电极,②电解质溶液或熔融电解质,③形成闭合回路
(4)阴离子放电顺序:S2->I->Br->Cl->OH->SO42->NO3->F- 阳离子放电顺序:Ag+>Hg2+>Fe3+>Cu2+>H+>Pb2+>Sn2+>Fe2+>Zn2+>Al3+>Mg2+>Na+>Ca2+>K+
(5)电解时溶液pH值的变化规律电解质溶液在电解过程中,有时溶液pH值会发生变化。判断电解质溶液的pH值变化,有时可以从电解产物上去看。
①若电解时阴极上产生H2(消耗H+),阳极上无O2产生,电解后溶液pH值增大;
②若阴极上无H2,阳极上产生O2,则电解后溶液pH值减小;
③若阴极上有H2,阳极上有O2,且(相当于电解水),则有三种情况:
a如果原溶液为中性溶液,则电解后pH值不变;
b如果原溶液是酸溶液,则pH值变小;
c如果原溶液为碱溶液,则pH值变大;
④若阴极上无H2,阳极上无O2产生,电解后溶液的pH可能也会发生变化。如电解CuCl2溶液(CuCl2溶液由于Cu2+水解显酸性),一旦CuCl2全部电解完,pH值会变大,成中性溶液。
(6)电解反应类型:从参加反应的物质来分电解反应可分成五类:
①H2O型:实质是电解水。如电解硝酸钠、氢氧化钠、硫酸等溶液。
②溶质型:溶质所电离出来的离子发生氧化还原,如电解氯化铜、溴化氢等溶液。
③硫酸铜溶液型:电解产物是金属、氧气与酸。如电解硫酸铜溶液生成单质铜、氧气和硫酸,电解硝酸银溶液时生成单质银、氧气和硝酸。
④氯化钠溶液型:电解产物是非金属单质、氢气与碱。如电解氯化钠溶液时生成氯气、氢气和氢氧化钠,电解溴化钾溶液时生成溴单质、氢气和氢氧化钾。
⑤电镀型:镀层金属作阳极,阳极反应是:M-ne-=Mn+,镀件作阴极,阴极反应是:Mn++ne-=M。(电解精炼与电镀,实质上是相同的)
电解的其他应用
电解的其他应用:
(1)电解CuSO4溶液
阴极:Cu2++2e-=Cu
阳极:4OH--4e-=O2↑+2H2O
总反应式:2Cu2++2H2O2Cu+O2↑+4H+
电解后溶液pH变小,加氧化铜可恢复原溶液
CuSO4溶液电解的实质:电解水和CuSO4
(2)电解Na2SO4溶液
阴极:2H++2e-=H2↑
阳极:4OH--4e-=O2↑+2H2O
总反应式:2H2O2H2↑+O2↑
Na2SO4溶液电解的实质:电解水
电解后溶液PH不变
高中化学电解池知识点
电解的原理
电解定义
在电流作用下,电解质在两个电极上分别发生氧化反应和还原反应的过程。
能量转化形式
电能转化为化学能。
电解池
构成条件
①有与电源相连的两个电极。
②电解质溶液(或熔融盐)。
③形成闭合回路。
分析电解过程的思维程序
首先判断阴、阳极,分析阳极材料是惰性电极还是活泼电极。
再分析电解质水溶液的组成,找全离子并分阴、阳两组(不要忘记水溶液中的H+和OH-)。
然后排出阴、阳两极的放电顺序
阴极:阳离子放电顺序:
Ag+>Fe3+>Cu2+>H+(酸)>Fe2+>Zn2+>H+(水)>Al3+>Mg2+>Na+>Ca2+>K+。
阳极:
活泼电极>S2->I->Br->Cl->OH->含氧酸根离子。
分析电极反应,判断电极产物,写出电极反应式,要注意遵循原子守恒和电荷守恒。
最后写出电解反应的总化学方程式或离子方程式。
电解原理的应用
电解饱和食盐水
电极反应
阳极反应式:2Cl--2e-=Cl2↑(氧化反应)
阴极反应式:2H++2e-=H2↑(还原反应)
总反应方程式
2NaCl+2H2O2NaOH+H2↑+Cl2↑
离子反应方程式:2Cl-+2H2O
2OH-+H2↑+Cl2↑
应用:氯碱工业制烧碱、氯气和氢气。
电镀
以金属表面镀银为例,
镀件作阴极,镀层金属银作阳极。
电解质溶液是AgNO3溶液等含镀层金属阳离子的盐溶液。
电极反应:
阳极:Ag-e-=Ag+;
阴极:Ag++e-=Ag。
特点:阳极溶解,阴极沉积,电镀液的浓度不变。
电解精炼铜
电极材料:阳极为粗铜;阴极为纯铜。
电解质溶液:含Cu2+的盐溶液。
电极反应:
阳极:
Zn-2e-=Zn2+
Fe-2e-=Fe2+
Ni-2e-=Ni2+
Cu-2e-=Cu2+;
阴极:
Cu2++2e-=Cu。
电冶金
利用电解熔融盐的方法来冶炼活泼金属Na、Ca、Mg、Al等。
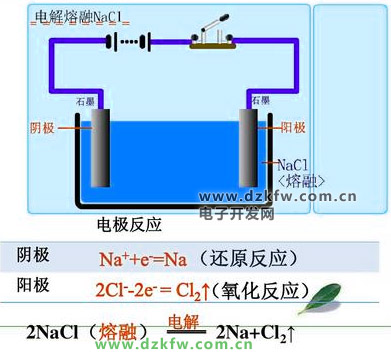
冶炼钠
2NaCl(熔融)电解2Na+Cl2↑
电极反应:
阳极:
2Cl--2e-=Cl2↑;
阴极:
2Na++2e-=2Na。
冶炼铝
2Al2O3(熔融)4Al+3O2↑
电极反应:
阳极:6O2--12e-=3O2↑;
阴极:4Al3++12e-=4Al。


 返回顶部
返回顶部 刷新页面
刷新页面 下到页底
下到页底