蓄电池通常用硫酸密度来衡量电解液的浓度。 充足电,密度1.26~1.28g/cm^3,相当于浓度是35~38% 完全放电:密度1.10~1.15,相当于浓度10~15% 充足电的电池,硫酸密度与稀硫酸原液浓度是一致的,因此把电解液倒出,再加上稀硫酸原液。
电瓶一般是铅酸蓄电池,它正常使用时,要求硫酸浓度,比重为1.27-1.28之间。使用过程中,不能亏电,否则两极板之间会生成硫酸铅结晶,它在于后的再充电过程就不能去除,成为死角。亏电时间久,生成的硫酸铅结晶多,电瓶就没用了。就不存电了。
铅酸蓄电池基本原理
铅酸蓄电池由若干对正、负极板相互交叠形成极群。
活性物质的量(由极板面积、厚度、极板对数量等因素决定)决定了贮存容量和电池容量。
此外,电池运行还显著的决定于“活性物质的有效活性表面”,因此,活性物质的孔隙率应经常考虑。
“accumulator”,来自拉丁语,表示“蓄电池”或“贮能蓄电池”。后面的意思经常使用。
通过化学和电化学反应,电池贮存能量。即,通过电化学过程产生电能,反之亦然。
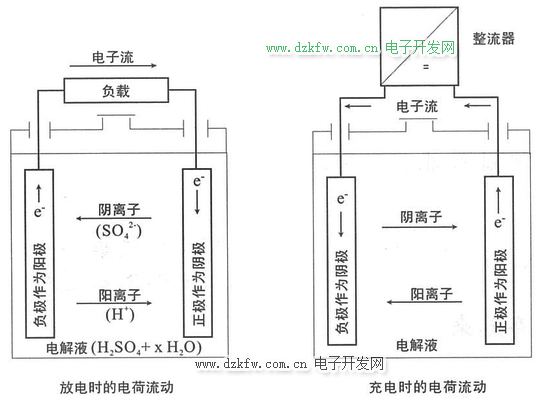
放电时:贮存的化学能转变成电能。
充电时:将电能以化学能的形式贮存起来。
铅酸蓄电池属于二次电池。(不同于原电池只能用于放电,不能充电)
电子:
放电时,当负载接通形成电流时,电子从负极(经负载)流向正极。
充电时,电子通过负极端子提供给电池。
在文献中往往剪刀相反的说法,即,放电时,电池外部的电流从正极流向负极,而充电时从负极流向正极。这个方向正好与电子流动的方向相反,被称为“工程上的电流方向”。按照作者的观点,电子流动的方向是“电流的实际方向”。这是本篇文章所描述过程的基础,两者不能混淆。
电子是带负电的质点。根据放电时从哪里提供电子,和充电时从哪里接受电子,最后规定电池端子(和极板)的称谓和标记。
标记“-”(或“Neg”或“N”)为负极端子,连接负极板(Negatives)。
标记“+”(或“Pos”或“P”)为正极端子,连接正极板(Positives)。





 返回顶部
返回顶部 刷新页面
刷新页面 下到页底
下到页底